FDA 21 CFR část 11: Sledovatelnost a ochrana proti neoprávněné manipulaci s výsledky zkoušek v testXpert
Nařízení 21 CFR část 11 (Code of Federal Regulations) o elektronických záznamech a elektronických podpisech Úřadu pro kontrolu potravin a léčiv Spojených států amerických (FDA) definuje kritéria používání elektronických záznamů a elektronických podpisů namísto záznamů v papírové podobě s vlastnoručními podpisy. S těmito elektronickými dokumenty se musí zacházet jako s důvěrnými, musí být stejně věrohodné a mít stejnou váhu jako dokumenty papírové.
Pro použití elektronických záznamů a podpisů v regulovaném prostředí je vyžadován soulad s předpisy FDA 21 CFR část 11 a směrnicemi EU GMP dodatek 11. Použití dokumentů v klasické papírové podobě a vlastnoručních podpisů je také možné.
testXpert nabízí skvělé řešení, které vám pomůže splnit požadavky FDA 21 část 11
- Zejména v medicínském a farmaceutickém průmyslu můžeme zaznamenávat vzrůstající požadavky kladené na používaný software, který dokumentuje sledovatelnost prováděných akcí.
- Volitelným doplňkem softwaru testXpert III je funkce sledovatelnost, která zaznamenává všechny aktivity a změny (před zkouškou, v jejím průběhu i po skončení zkoušky), aby byly výsledky i dokumentace sledovatelné a zároveň je chrání před možnou manipulací.
- Integrovaná správa uživatelů a funkce jako elektronický záznam a podpis zajišťují, že s výsledky zkoušek nelze manipulovat.
- Spolu s organizačními opatřeními a procedurálními pokyny, které platí v jednotlivých organizacích, jsou splněny požadavky podle FDA 21 CFR část 11.
- ZwickRoell navíc nabízí servisní balíček pro kvalifikaci (DQ/IQ/OQ) pro podporu validace.
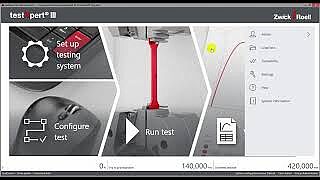
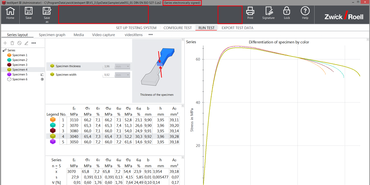
- testXpert III zaznamenává veškeré akce nastavení systému a zkoušek, a proto může vždy odpovědět na otázku:
„Kdo udělal co, kdy, proč a kdo nese odpovědnost?“
Zkoušky kritické z hlediska bezpečnosti
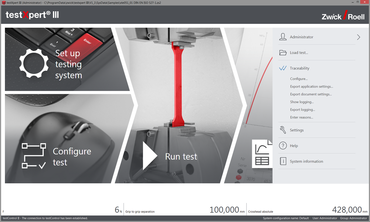
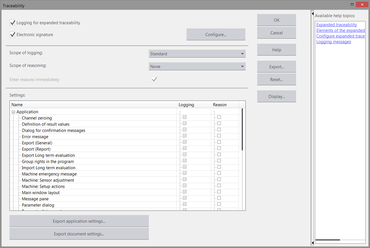
Předvolby rozšířené sledovatelnosti lze konfigurovat podle potřeby a stupně sledovatelnosti. Administrátor definuje, co se musí zaznamenat a pro které činnosti nebo události musí uživatel zadat důvod. Tímto způsobem nabízí testXpert III zákazníkům možnost individuální adaptace podle předpisů QS.
Elektronické záznamy
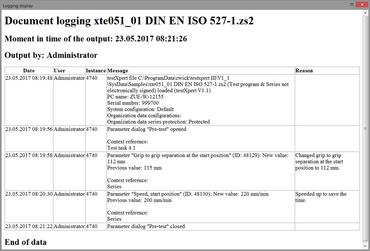
Funkce elektronických záznamů umožňuje kompletní a proti neoprávněné manipulaci chráněnou dokumentaci všech akcí či změn provedených v testXpert III. Uživatelé definují, do jaké míry musí být akce zaznamenány a případně vysvětleny v souladu s jejich regulačními požadavky (například změny relevantních zkušebních parametrů, jako rychlost zkoušky). Tyto údaje jsou uloženy v auditovaném záznamu.
- Protokolované záznamy jsou ukládány do systémové auditní stopy nebo do příslušných souborů (programy, série zkoušek) automaticky a nezávisle na typu.
- Data jsou uložena v binárním formátu a nelze je editovat pomocí standardních programů Windows.
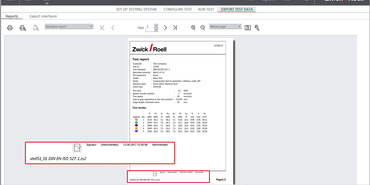
- Výstup lze kdykoli vygenerovat v „čitelné“ podobě (HTML / PDF) v programu testXpert III.
- Záznamy protokolování jsou archivovány v zašifrované podobě.
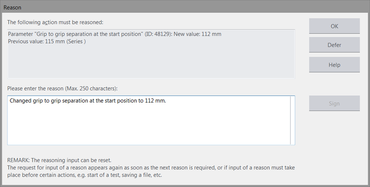
- Volitelný důvod se automaticky přidá do příslušného protokolu (se starou a změněnou hodnotou).
- Komentáře lze do auditovaného záznamu vkládat v dialogovém okně nabídky.
Elektronický podpis
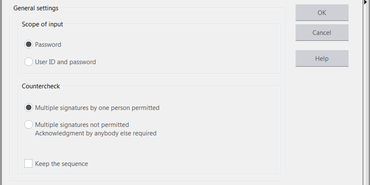
Modul Elektronický podpis také spolehlivě chrání zkušební program / série zkoušek před nežádoucími změnami. Umožňuje tak dokumentovat, kdo přebírá odpovědnost a zároveň zajišťuje digitální auditovaný záznam. Podpis na zkušebním protokolu v souboru s programem nebo sérii zkoušek může být nahrazen digitálním podpisem – zadáním uživatelského jména a hesla v softwaru. Je možné definovat, kolik osob musí protokol podepsat a kdo k tomu má oprávnění. Po tomto podpisu jsou soubory se zkušebním programem nebo sérií zkoušek chráněny proti neoprávněným změnám.
Kvalifikace strojů a přístrojů pro zkoušení materiálů
Významným prvkem validace procesů ve zdravotnictví a farmaceutickém průmyslu je technická revize jednotlivých zařízení a přístrojů. Tato kvalifikace je vyžadována také pro systémy ZwickRoell pro zkoušení materiálů používaných v lékařském a farmaceutickém průmyslu, protože systémy podléhají různým právním požadavkům (například podle Směrnice o zdravotnických zařízeních 93/42/ES nebo předpisům jako je FDA 21 CFR část 11).
Společnost ZwickRoell provádí kvalifikaci systémů pro zkoušení materiálů v procesech DQ (kvalifikace návrhu), IQ (kvalifikace instalace) a OQ (provozní kvalifikace) tím, že nabízí komplexní nebo individuální kvalifikační dokumentaci, jakož i praktické provedení kvalifikace na místě.