FDA 21 CFR Part 11: Identyfikowalne i zabezpieczone przed manipulacją wyniki badawcze z testXpert
Zapis FDA 21 CFR Part 11 (Code of Federal Regulations) amerykańskiej Agencji ds. Żywności i Leków (Food and Drug Administration), dotyczący „Zapisów elektronicznych i podpisów elektronicznych” określają kryteria akceptacji stosowania zapisów elektronicznych (electronic records) i podpisów elektronicznych (electronic signatures) zamiast zapisów w formie papierowej i odręcznych podpisów na papierze. Te dokumenty elektroniczne muszą być tak samo godne zaufania, rzetelne i mieć taką samą wartość jak poprzednie dokumenty papierowe.
W przypadku korzystania z zapisów elektronicznych i podpisów w środowisku regulowanym wymagana jest zgodność z FDA 21 CFR Part 11 i załącznikiem 11 do przewodnika UE GMP. Nadal możliwe jest korzystanie z tradycyjnych dokumentów papierowych i podpisów odręcznych.
Oprogramowanie badawcze testXpert oferuje idealne rozwiązanie zapewniające zgodność z FDA 21 Part 11
- W szczególności w branży farmaceutycznej i technologii medycznej rośnie zapotrzebowanie na oprogramowanie, które dokumentuje możliwość rozszerzonego śledzenia przeprowadzonych działań.
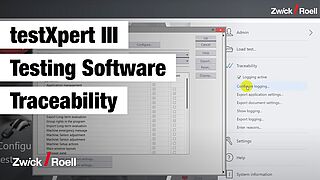
- Opcja „Weryfikowalność” w oprogramowaniu testXpert III umożliwia ewidencjonowanie wszystkich operacji i zmian - przed, w trakcie oraz po wykonaniu badania -, co pozwala na weryfikację i zabezpieczenie przed manipulacją wyników badań oraz dokumentacji.
- Zintegrowany moduł „Zarządzanie użytkownikami” oraz takie funkcje jak „Ewidencjonowanie elektroniczne” oraz „Sygnatura elektroniczna” gwarantują pełne zabezpieczenie wyników badania przed manipulacją.
- W ten sposób oraz przy uwzględnieniu działań organizacyjnych i zaleceń proceduralnych obowiązujących w danej firmie spełniamy wymogi zawarte w ustawie FDA in 21 CFR Part 11.
- Jako uzupełnienie ZwickRoell oferuje dodatkowy pakiet serwisowy Pakiet usług kwalifikacyjnych (DQ/IQ/OQ) wspierający walidację badań.
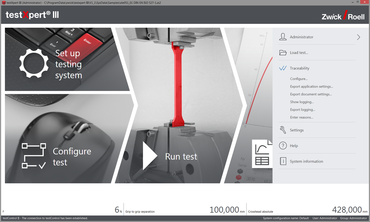
- testXpert III rejestruje wszystkie działania i ustawienia związane z badaniem i systemem, a tym samym dostarcza odpowiedzi na pytanie w dowolnym momencie
„Kiedy kto, co robi, dlaczego i kto jest odpowiedzialny?“
Badania krytyczne dla bezpieczeństwa
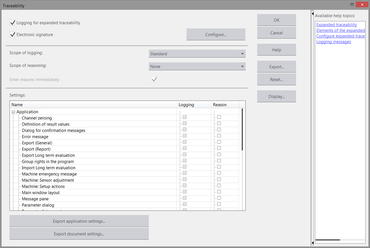
Opcję „Rozszerzonego śledzenia“ można dowolnie konfigurować. Przy czym można także określić stopień rozszerzonego śledzenia. Odpowiedzialny organ określa zatem, co jest rejestrowane i dla jakich procesów i zdarzeń użytkownik musi podać przyczyny. TestXpert III oferuje więc możliwość indywidualnego dostosowania się do zasad QS w środowisku klienta.
Zapisy elektroniczne
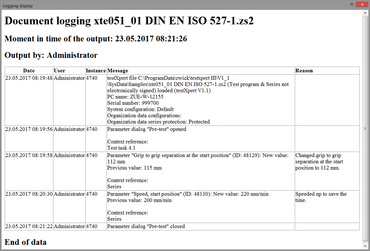
Funkcja „Zapisu elektronicznego” umożliwia pełną, niemożliwą do zmanipulowania dokumentację wszystkich działań i zmian dokonanych w testXpert III. Użytkownik określa poziom działań, które mają być rejestrowane i ewentualnie uzasadniane zgodnie z jego wymogami regulacyjnymi (np. zmiana parametru istotnego dla badania, takiego jak prędkość badawcza). Dane te zapisywane są w pliku transkrypcji (Audit-Trail).
- Wpisy dziennika są zapisywane automatycznie i w zależności od typu w ścieżce audytu systemu ewentualnie w odpowiednim programie/serii badawczej.
- Dane przechowywane są w formie binarnej i nie można ich zmieniać za pomocą standardowych programów Windows.
- Dane wyjściowe można w dowolnym momencie utworzyć w „czytelnej” formie (HTML / PDF) z testXpert III.
- Dane transkrypcji są archiwizowane w formie zaszyfrowanej.
- Opcjonalne uzasadnienie jest automatycznie dodawane do odpowiedniego wpisu dziennika (ze starą i zmienioną wartością).
- Dowolny komentarz można wstawić do Audit-Trail za pomocą punktu menu.
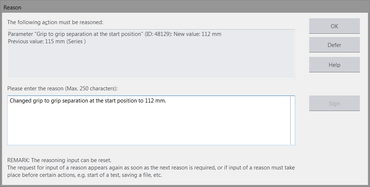
Podpis elektroniczny
Funkcja „Podpisu elektronicznego“ niezawodnie chroni także program badania/serię badawczą przed niepożądanymi zmianami. Podpis umożliwia udokumentowane przejęcie odpowiedzialności i tym samym przejście na „dokumentację bez papieru”. Podpis na protokole badawczym można zastąpić podpisem elektronicznym programu badania/serii badawczej, wprowadzając identyfikator użytkownika i hasło w oprogramowaniu badawczym. Możesz dokładnie określić, ile osób ma się podpisać i kto jest do tego upoważniony. Program badania i seria badawcza są chronione przed nieuprawnioną zmianą statusu podpisu.
Kwalifikacja maszyn i urządzeń do badania wytrzymałości materiałów
Istotną częścią walidacji procesów w technologii medycznej i przemyśle farmaceutycznym jest kontrola techniczna poszczególnych systemów i urządzeń. Kwalifikacja ta jest również wymagana w przypadku systemów do badania wytrzymałości materiałów ZwickRoell stosowanych w technologii medycznej i przemyśle farmaceutycznym, ponieważ podlegają one różnym wymaganiom prawnym (np. zgodnie z dyrektywą dotyczącą wyrobów medycznych 93/42/EWG lub przepisami takimi jak FDA 21 CFR Part 11).
ZwickRoell wspiera Cię w kwalifikacji systemów badawczych ZwickRoell na etapach DQ (kwalifikacja projektowa), IQ (kwalifikacja instalacyjna) i OQ (kwalifikacja funkcjonalna) w formie kompleksowej i na żądanie, indywidualnie dostosowanej dokumentacji kwalifikacyjnej, a także w przeprowadzanie kwalifikacji w miejscu użytkowania.