FDA 21 CFR Part 11: testXpert를 이용한 추적이 가능하고 조작이 불가능한 시험 결과
미국식품의약국(Food and Drug Administration, FDA)의 전자 기록 및 전자 서명에 관한 FDA 21 CFR Part 11(미국연방기준집[Code of Federal Regulations]) 규정에서는 서면 양식 및 서면상의 수기 서명 대신 전자 기록 및 전자 서명을 사용하는 허용 기준을 정의하고 있습니다. 이러한 전자 문서는 기밀로 취급해야 하며, 서면과 동일한 가치를 지닙니다.
규정 FDA 21 CFR Part 11 및 EU GMP 가이드라인 부록 11은 규제된 환경에서의 전자 기록 및 서명 사용에 필요합니다. 기존의 종이 문서와 수기 서명은 계속 사용할 수 있습니다.
testXpert는 FDA 21 Part 11 요건을 충족할 수 있는 완벽한 솔루션입니다.
- 의료 및 제약 업계의 경우 수행 완료된 행위를 추적할 수 있는 소프트웨어에 대한 수요가 그 어느 때보다 계속 증가하고 있습니다.
- 추적 가능성 옵션이 있는 testXpert III는 시험 전, 시험 중, 시험 후의 모든 조치와 변화를 기록하므로 시험 결과값과 작성된 문서를 추적할 수 있으며 조작을 방지합니다.
- 전자 기록과 전자 서명 같은 사용자 관리와 기능이 내장되어 있어 시험 결과를 위조의 위험으로부터 항상 보호되고 있습니다.
- 기업별 관리적 보호조치 및 절차 지침과 더불어 21 CFR Part 11의 FDA 요구사항을 준수합니다.
- ZwickRoell은 유효성 확인을 위한 적격성 평가 서비스 패키지(DQ/IQ/OQ)도 제공하고 있습니다.
- testXpert III는 시험 및 시스템 관련 작업과 설정을 모두 기록하기 때문에 항상 질문에 답할 수 있습니다.
“누가 언제 무엇을 왜 했으며, 책임자는 누구인가?”
전자 기록
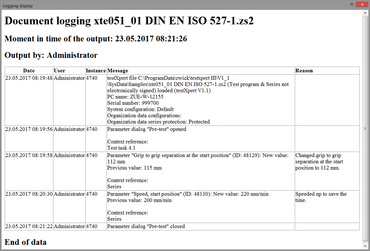
전자 기록 기능을 통해 testXpert III에서 수행되는 모든 작업과 변경 사항을 완전하고, 조작 불가능하게 문서화할 수 있습니다. 사용자는 규정 요건에 따라 작업을 기록하고 설명해야 하는 정도를 정의합니다(예: 시험 속도 같은 시험 매개변수 변경). 이 데이터는 감사 추적에 저장됩니다.
- 기록 항목은 시스템 감사 추적 또는 관련 시험 프로그램/시리즈의 유형과는 별개로 자동 저장됩니다.
- 데이터는 2진 부호로 저장되며 Windows 규격 프로그램으로는 편집할 수 없습니다.
- 출력은 testXpert III에서 언제든 “읽기 가능한” 형식(HTML/PDF)으로 생성할 수 있습니다.
- 기록된 데이터는 암호화된 형식으로 보관됩니다.
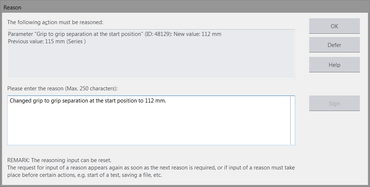
- 이유(옵션)가 해당 보고서 입력에 자동으로 추가됩니다(이전 값과 수정 값 포함).
- 메뉴 항목을 통해 감사 추적에 의견을 입력할 수 있습니다.
재료 물성시험기 및 설비 적격성 평가
의료 엔지니어링 및 제약 산업의 공정 유효성 확인에서 중요한 요소는 개별 공장과 장치에 대한 기술 검토입니다. 여러 시스템에 다양한 법적 요구사항(예: 의료기기 지침 93/42/EEC 또는FDA 21 CFR Part 11 같은 규정)이 적용되기 때문에 의료 및 제약 업계에서 사용하는 ZwickRoell 재료 물성시험 시스템도 동일한 자격이 요구됩니다.
ZwickRoell은 DQ(설계 적격성 평가), IQ(설치 적격성 평가), OQ(운영 적격성 평가) 절차에서 재료 물성시험기 시스템의 적격성 평가를 지원합니다. 이를 위해 요청에 따라 개별 맞춤형 종합 적격성 평가서를 제공하고, 현장에서 실제 적격성 평가를 진행합니다.